AD血液生物标志物在全球医疗保健格局变换下的现状与前景
发布日期:2024-01-04点击量:929次编辑:szbyjy_admin
以下文章来源于生物标志物研究 ,作者QiQi Zeng
01
研究背景
02
研究内容
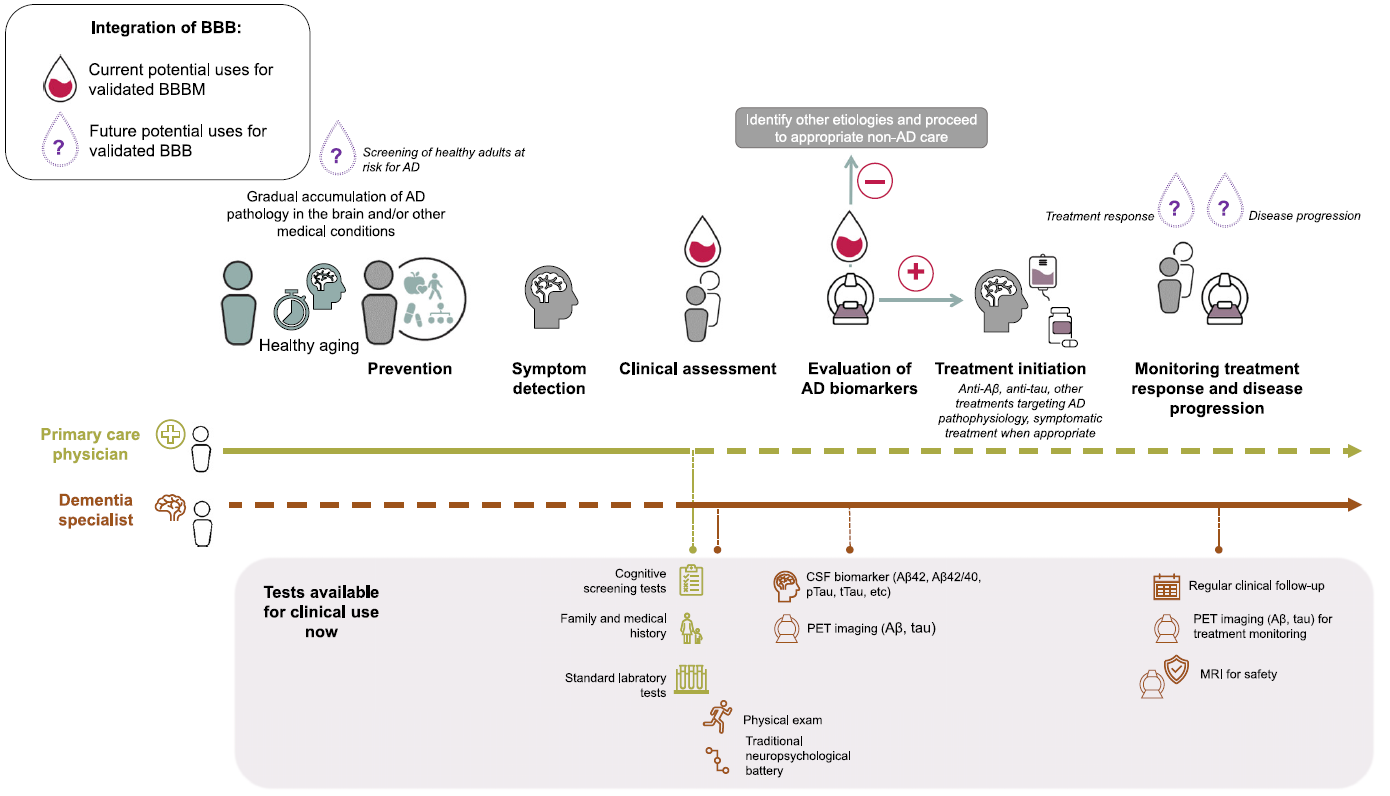
03
研究结论
04
参考文献
免责声明:本公众号发布内容部分信息来源网络,旨在学习交流与分享,所发表内容注明来源的,版权归原出处所有,与本公众号立场无关;无法查证版权的或未注明出处的均来源于网络搜集;如存在不当使用或侵权的情况请联系后台删除。
上一篇:七项呼吸道感染病原体IgM抗体检测的临床意义
下一篇:化学发光技术原理









 苏公网安备32050502011778号
苏公网安备32050502011778号



